
1、残留溶剂的影响
1.1、安全风险:Class 1溶剂(如苯)具强致癌性;Class 2溶剂(如甲醇)有生殖毒性;Class 3溶剂(如丙酮)低毒但过量影响产品纯度。
1.2、工艺稳定性:残溶可能改变结晶行为、引发降解(如水解反应),导致晶型不一致或杂质超标。
1.3、法规要求:ICH Q3C明确三类溶剂限值(Class 1:2-10ppm;Class 2:50-2500ppm;Class 3:5000ppm)。
2、水分的影响
2.1、化学稳定性:水分催化水解反应(如阿司匹林水解为水杨酸和乙酸),加速API降解。
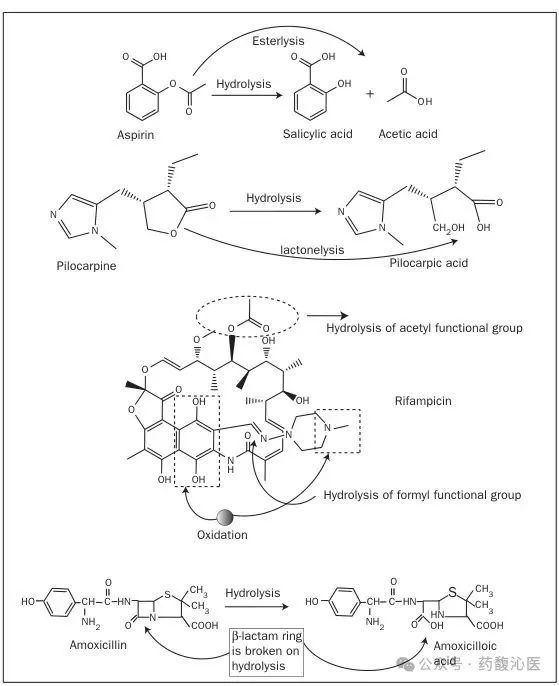
2.2、物理性质:水分过高导致结块、流动性差,影响压片或分装。
2.3、微生物风险:>1%水分可能滋生微生物。
1、工艺耐受性评估:模拟极端条件(如杂质超标、水分波动),验证工艺能否维持质量属性。
2、杂质清除能力量化:通过"去除因子"(加标杂质去除率)制定物料标准。
3、控制限度合理性证明:为质量标准提供数据支持。
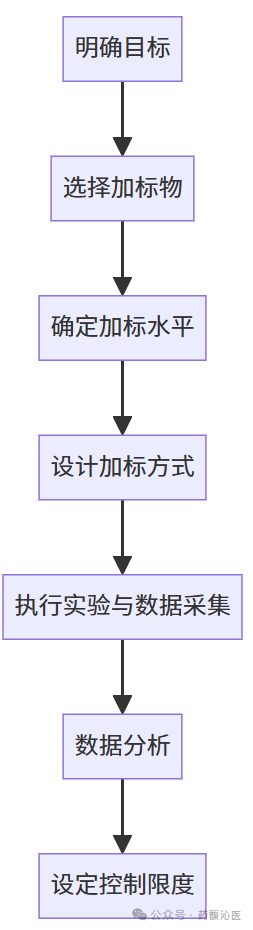
1、选择加标物
1.1、残溶:优先选择工艺中实际使用的溶剂及其潜在降解产物(如甲苯中残留苯)。
1.2、水分:直接加入纯化水或高水分物料。
1.3、杂质:富集原料中已知杂质或合成模拟物(若无标准品)。
2、确定加标水平
2.1、基准值:日常检测值的1.5-5倍(如检出杂质0.10% → 加标至0.2-0.5%)。
2.2、上限原则:不超过工艺承受极限(避免反应中止),且需覆盖ICH限值的120%。
2.3、水分加标:通常在0.5%-5%范围内梯度设计。
3、加标方式
3.1、零点加标:反应前将加标物与底物混合溶解(HPLC监测起始点)。
3.2、过程加标:在关键步骤(如结晶前)加入,模拟意外污染。
3.3、注意事项:
3.3.1、多杂质需共存加标(避免独立加标导致虚假结论)。
3.3.2、确保均匀混合(如超声处理、机械搅拌)。
4、数据采集与分析
4.1、关键指标:
参数
检测方法
评价指标
残溶去除率
GC-FID/顶空GC
各溶剂残留量 vs ICH限值
水分影响
Karl Fischer滴定
降解产物增长率、晶型变化
杂质去向
HPLC-MS
去除因子=(加标量-终残量)/加标量
去除因子应用:若工艺去除因子≥90%,可放宽起始物料标准。
1、直接引用ICH Q3C限值(如Class 2溶剂甲醇限值3000ppm)。
2、基于工艺能力修正:
2.1、加标实验显示工艺可稳定将甲醇降至100ppm → 内控限度可设为150ppm(留出安全余量)。
3、豁免场景:若证明Class 1溶剂(如苯)在工艺中被完全清除,可免除常规检测(需提供配方、流程、稳定性数据)。
1、稳定性导向:
1.1、加速试验(40℃/75%RH)中水分≤1%时API降解<0.2% → 限度设为1.0%。
2、工艺需求:
2.1、湿法制粒要求水分2-4%,而直接压片需≤0.5%。
3、参比原研:原研药水分0.8% → 仿制药限度定为≤1.0%。
背景:合成中使用甲醇(Class 2),需控制终产品残溶。
加标实验:
加标水平:甲醇加标至4000ppm(ICH限值3000ppm的133%)。
结果:经结晶纯化后残留量稳定在200±50ppm。
限度设定:
ICH限值3000ppm → 内控标准定为1000ppm(预留5倍安全余量)。
背景:阿司匹林易水解,水分需严格管控。
加标实验:
梯度设计:水分加标至1.0%、1.5%、2.0%。
结果:水分≥1.5%时,加速试验1月降解率>0.5%(超标)。
限度设定:根据稳定性数据定限度为≤1.0%。
背景:钯催化反应对水分敏感,需制定原料水分标准。
加标实验:
向反应体系加入0.1%、0.3%、0.5%水。
结果:水分>0.3%时催化剂失活,转化率下降>20%。
限度设定:原料水分限度≤0.2%。
1、实验时机:工艺参数锁定后进行加标,避免数据失效。
2、数据分析严谨性:需计算置信区间(如95%CI),确保限度可靠性。

异常数据处理:若加标后反应中止,需降低加标量重新实验。
3、方法验证:加标回收率需达80-120%。
4、文件记录:保存加标浓度、样品均一性证明、原始色谱/光谱数据。
加标实验是衔接工艺开发与质量标准的核心工具:
操作要点:以工艺耐受性为基准设计加标水平,通过共存加标模拟真实场景,量化去除因子支持限度制定。
限度逻辑:ICH限值为底线,结合工艺能力、稳定性及原研数据收紧内控标准。
持续优化:工艺变更后需重新加标验证,确保控制策略持续有效。