
本文为转化医学网原创,转载请注明出处
作者:Walter
导言:随着新冠肺炎掀起轩然大波,全球死亡人数已达92391人,仍呈现恐怖的直线上升趋势,国外惊恐的群众对待这场“瘟疫“的解药有如期盼神迹降临。但是药物研发从来不能一蹴而就,前段时间被奉为“人民的希望”的瑞德西韦就是针对埃博拉病毒、研发了13年但最终无效的药物,关于其治疗新冠病毒的安全性、疗效的定论还遥遥无期。在新药“远水不解近渴”的情况下,中国学者决定另辟蹊径:老药新用!
4月9日,Nature加速发表了中科院上海药物所、清华大学和上海科技大学的三位大牛蒋华良院士、饶子和院士和杨海涛研究员团队的重要工作。研究者锁定COVID-19的新靶点Mpro蛋白酶,通过结构辅助药物设计、计算机虚拟筛选和高通量筛选手段,在FDA批准的已上市和临床实验药物中发现镇痛「老药」依布硒啉对Mpro具有o强烈的结合能力,并在细胞实验中展现出优异的抗病毒效果。

COVID-19的基因组由大约30000个核苷酸组成,其重组酶编码的两个重叠多蛋白,pp1a和pp1b,是病毒的复制和转录所必需的;长度为33.8 kDa的主要蛋白酶Mpro所介导这两个多蛋白11个位点以上的水解和断裂,释放出一系列功能各异的多肽,以维系病毒的生命活动。鉴于Mpro与人类蛋白的低同源性,不像ACE2酶在那样人体广泛表达, 靶向Mpro蛋白酶似乎是不会误伤人体细胞的、病毒特异性的可靠的抗病毒手段。
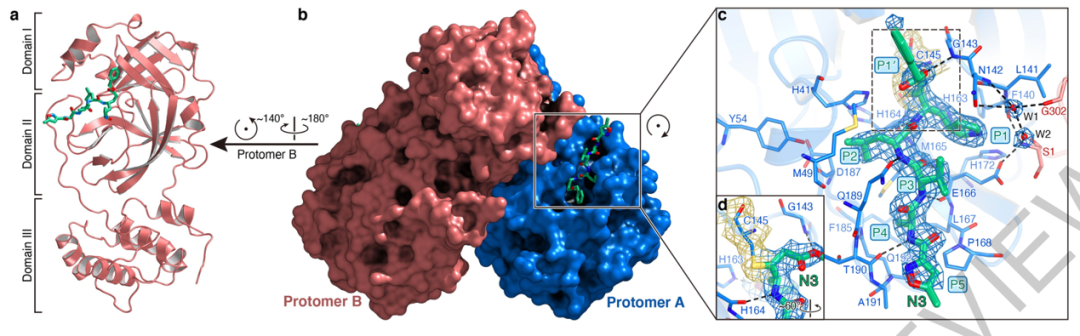
COVID-19 Mpro蛋白酶与N3结合物晶体结构
在此前的研究中,研究者通过计算机辅助设计了多种冠状病毒Mpro蛋白酶的抑制剂,N3。通过衍射电镜观察结合物的晶体结构,研究者发现COVID-19与Mpro抑制剂能牢固、不可逆地结合,这和N3与SARS-CoV的底物结合口袋和结合方式十分相似,提示该位点可能是抗冠状病毒的广谱靶点。
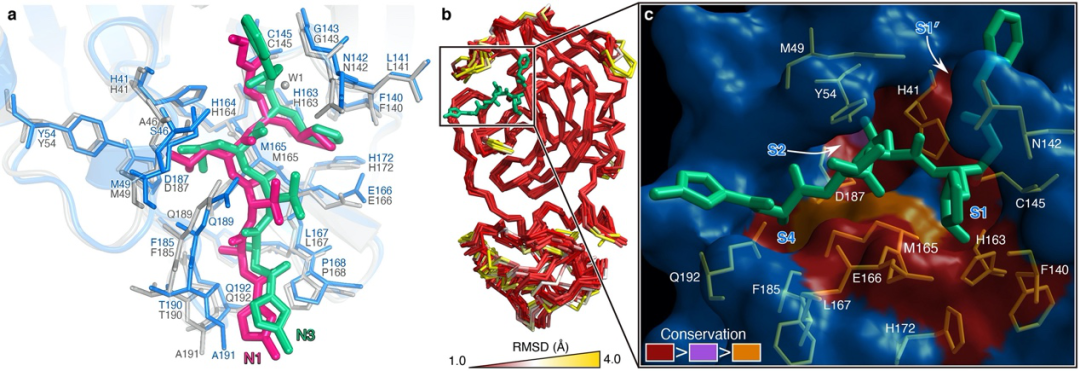
不同冠状病毒底物结合口袋
接着,研究者们在约10000个已批准药物、临床实验药物、候选化合物和天然产物中进行高通量筛选,并限定适合成药的条件为半数有效剂量IC50为0. 67 to 21.4 μM ,最终确定了6个潜在的候选药物,其中戒酒药双硫仑(disulfiram)和抗肿瘤药卡莫氟(carmofur)为FDA批准药物,而依布硒啉(ebselen)、紫草醌(shikonin)、tideglusib、PX-12和TDZD-8为临床和临床前实验药物。其中,依布硒啉的Mpro蛋白酶抑制效果最强。
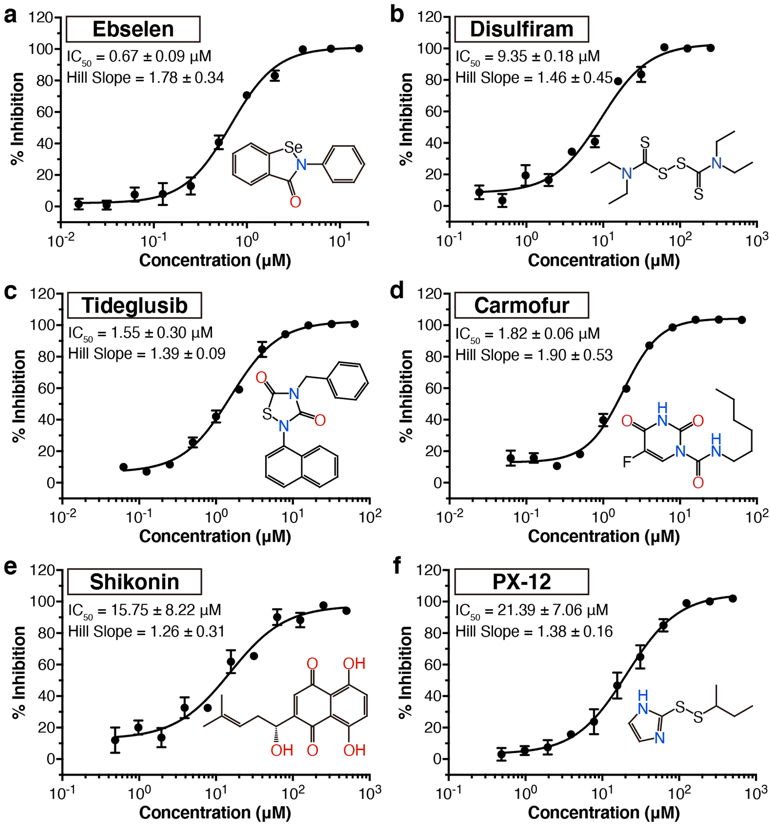
不同先导药物对COVID-19 Mpro蛋白酶的抑制效果
依布硒啉谷是一种具有谷胱甘肽过氧化酶活性的小分子有机硒化合物,自20世纪80年代以来,其在炎症、听力丢失以及中风、双向情感障碍和遗传性运动神经元疾病中的作用先后被解锁。依布硒啉位于美国国立卫生院(NIH)下属的临床药物库中,其人体安全性已被多次证明,囿于种种原因没能成功上市,因此抗新冠病毒可能成为它的新使命。
最后,研究者对COVID-19感染的Vero细胞施用依布硒啉,发现其在浓度为10 nM时便显示出强大的抗病毒作用。依布硒啉能穿透细胞膜以攻击病毒,与N3相比,其半数有效时所需剂量更低,还具有抗炎、抗氧化和细胞保护作用,考虑到它已经通过了临床一期实验,在抗COVID-19方面具有无与伦比的优势和前景。
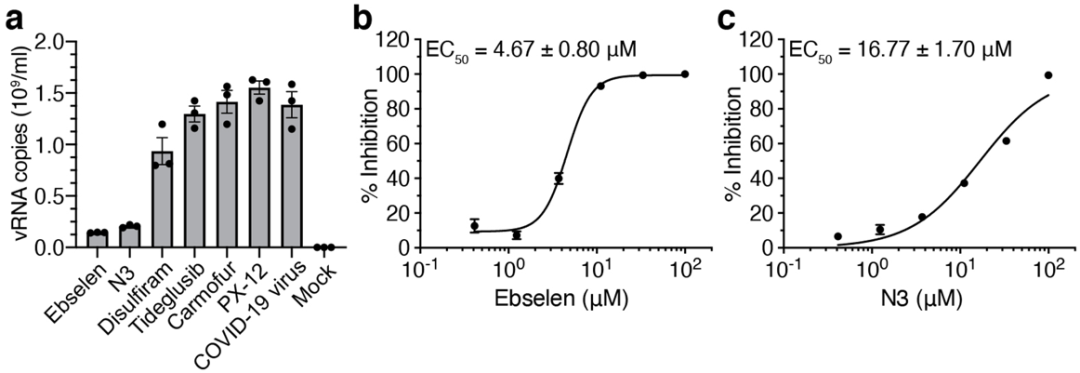
依布硒啉和N3的抗病毒活性
研发新药通常需要十数年时间以及数以亿计的金钱,其中传统的生物实验更添一份繁冗而严格的评价过程,因此在如此紧迫的情势下研制出抗COVID-19的新药几乎是天方夜谭。中国院士带领的一批学者采用最新的计算机辅助药物设计和筛选的手段,摒弃热点ACE2,发掘新靶点Mpro蛋白酶,并成功地筛选出6个能直接用于人体的化合物,尤其提出“种子选手”依布硒啉。这一发现堪称壮举,犹如为驱散世界疫情的阴霾率先点燃了一把火炬,是真正的“人民的希望”!
参考文献:
https://www.nature.com/articles/s41586-020-2223-y_reference.pdf