
2022年1月14日,Glenmark Pharmaceuticals 宣布获得美国 FDA 对 Ryaltrais 的新药申请( NDA )的批准。
Ryaltris是美国Glenmark全资子公司Glenmark Speciality S.a.(瑞士)的一种固定剂量处方药产品,用于治疗12岁以上成人和儿童季节性变应性鼻炎症状。该公司获得了Ryaltris的NDA批准。
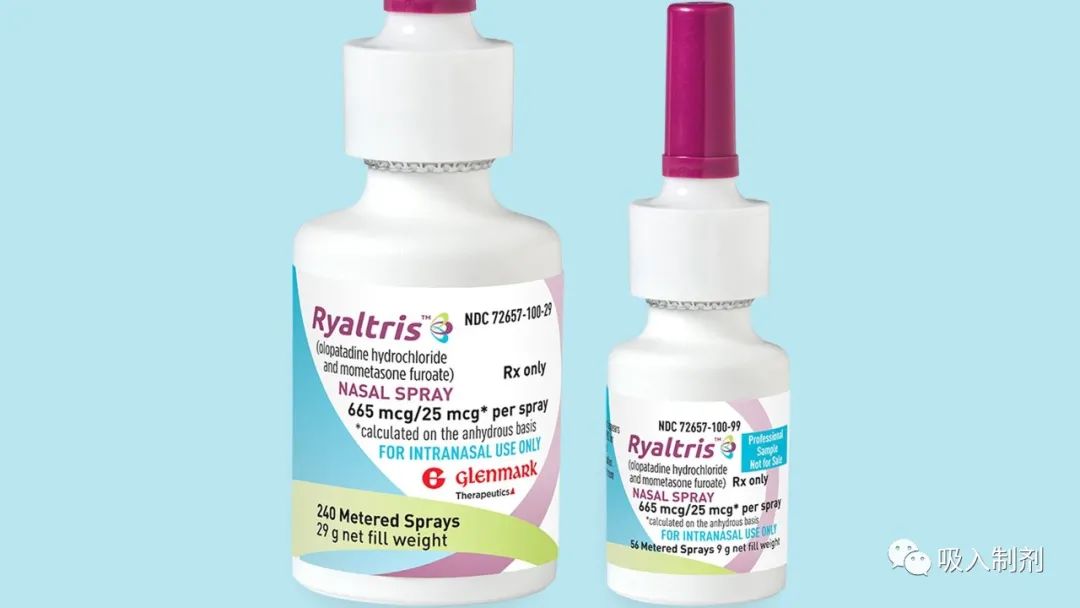
每单位水性悬浮鼻喷雾剂含有665微克盐酸奥洛他定(组胺-1(H1)-受体抑制剂)和25微克糠酸莫米松(皮质类固醇)。Ryaltris的推荐日剂量是每天两次在每个鼻孔喷两次。
Ryaltris在澳大利亚、捷克共和国、波兰、俄罗斯、南非、乌克兰、英国和乌兹别克斯坦获得批准。Hikma
Speciality U.S.A.将在美国营销和分销Ryaltris,作为与Glenmark Speciality S.A.签订的独家许可协议的一部分。
“ FDA 对 Ryaltris 的批准代表了 Glenmark 的一个重要里程碑,并明确支持我们为我们的关键治疗领域带来创新治疗选择的努力,” Glenmark Pharmaceuticals 的 CCO Robert
Crockart 在新闻稿中说。“通过这项 NDA 批准,我们期待将这种新药带给医生和他们的患者,用于治疗季节性过敏性鼻炎的症状,包括鼻部和眼部症状。”


